De 5 belangrijkste aandachtpunten over anodes
1. Gebruik het juiste materiaal voor uw vaarwater. Waar ligt de boot?
o Zink voor langdurig gebruik in zout water
o Aluminium als milieuvriendelijker alternatief voor zout en brak water
Maar let op: deze zullen sneller op gaan en vervangen moeten worden
o Magnesium enkel voor zuiver zoet water, denk aan Noorse bergmeren
2. Gebruik geen verschillende anodematerialen op 1 boot, de ene anode offert dan zichzelf op als anode voor de andere.
3. Er moet verbinding gemaakt worden via de metalen strip, niet via de achterkant met werkzaam materiaal. Oplossingen hiervoor zijn:
- Afstand houden tot de romp d.m.v. boutverbinding
- Achterzijde voorzien van verf
- Gebruik een rubberen pakking
4. Voorkom zowel onderprotectie (anodes gaan te snel op) als overprotectie (aantasting verfsysteem)
5. Vervang op tijd. Dat anodes er nog goed uit zien betekent niet dat werking nog goed is, de werkzame stof kan al verdwenen zijn

Waar kunnen anodes nodig zijn?
Rond of op de schroefas
Op de boegschroef of het staartstuk
In de boiler
Op de romp of het roerblad
Ga voor de juiste bescherming van uw metalen aan boord! Bekijk ons assortiment met zo’n 2000 verschillende anodes. Veel daarvan zijn uit voorraad leverbaar.
— Jos Boone Watersport
Waarom heb je anodes nodig? Hoe werkt dat ook alweer met elektrolyse?
Hieronder een simpele uitleg over de werking van opofferingsanodes.
Anodes gebruik je voor kathodische bescherming, daarom worden het opofferingsanodes genoemd.
Dit is vooral nodig in het geval van metaal onder water wat je wil beschermen tegen corrosie. Het is eigenlijk een natuurlijk proces waarbij gebruik gemaakt wordt van het potentiaalverschil tussen de opofferingsanode en het te beschermen metaal, de kathode. Doordat het potentiaal van de (legering van de) anode lager is dan de meeste metalen aan boord kan er een elektrochemische proces plaatsvinden. Het potentiaalverschil wordt geëgaliseerd door een stroom die van de anode naar de kathode vloeit. Hierbij verliest de anode elektronen en lost er materiaal op in water. De kathode (het metaal) behoudt dan elektronen en daar wordt corrosie voorkomen.
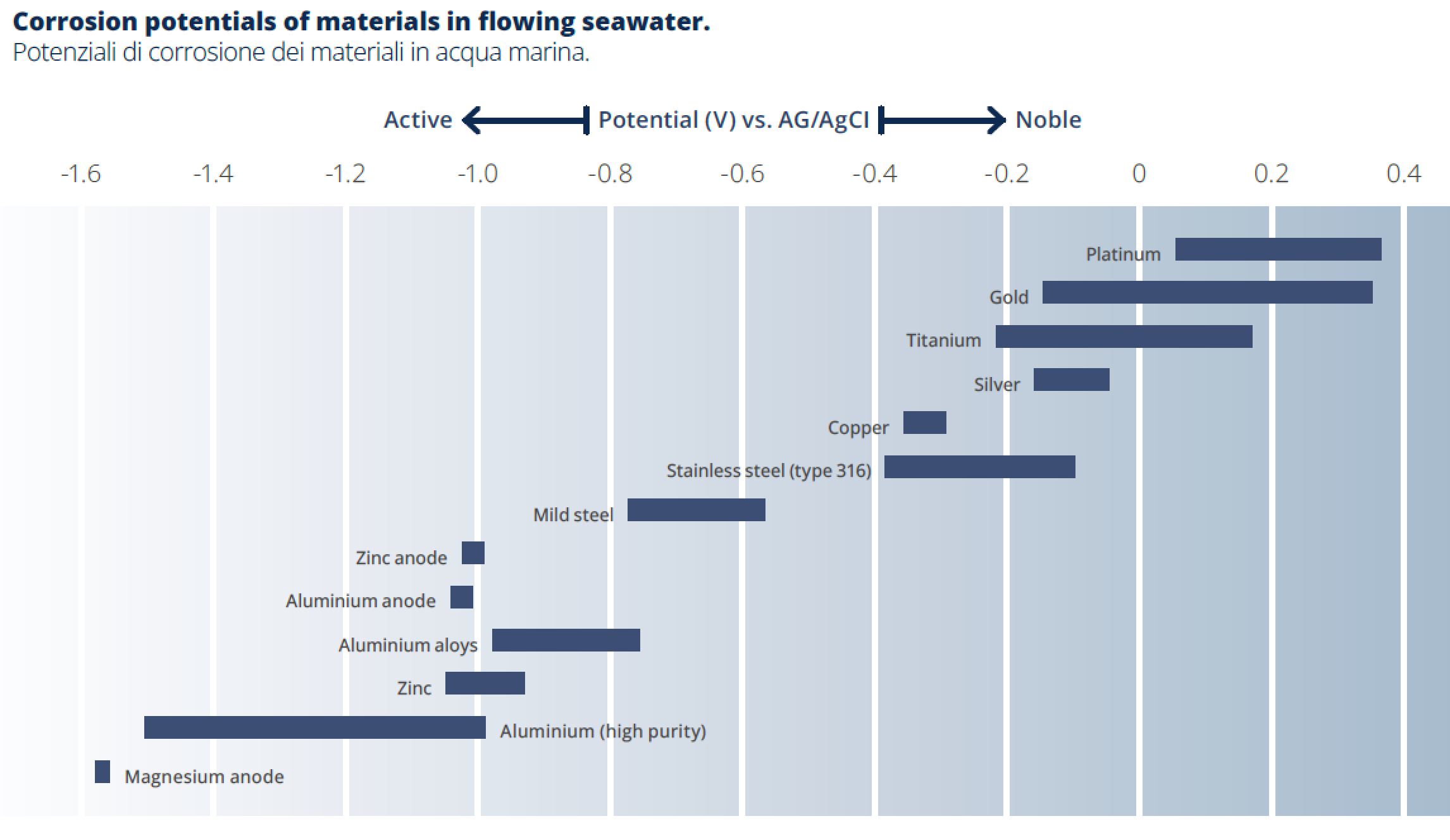
De meeste metalen gaan corroderen in water maar niet allemaal even makkelijk. Dat heeft te maken met de edelheidsreeks. Hoe lager op de schaal, hoe sneller de galvanische corrosie. Daarnaast is de onderlinge afstand op de schaal ook van invloed op hoe sterk de reactie zal zijn.
Bron: Tecnoseal Catalogus 2026
Op de schaal is ook goed te zien waarom we meestal geen magnesium anodes adviseren, die verliezen vaak te snel hun materiaal omdat het potentiaalverschil zo groot is. Die zijn alleen geschikt voor zuiver zoet water waar de mate van elektrolyse minder is.
Daarnaast wordt duidelijk waarom aluminium een vervanger kan zijn voor zink, er is namelijk best wat overlap op de schaal. Let dan wel op dat aluminium wel sneller ‘op’ zal zijn en vervangen moet worden. Een voordeel van aluminium ten opzichte van zink is dat de vrijgekomen stof minder schadelijk is voor het milieu.
Een aluminium anode is niet van hetzelfde aluminium gemaakt als het aluminium waar ook boten van gemaakt worden. Een anode bestaat namelijk uit meerdere materialen die tijdens het proces weer van elkaar gescheiden worden en die samen zorgen voor de werking. In veel anodes is bijvoorbeeld staal verwerkt wat ervoor zorgt dat de anode niet direct los laat van de plek van montage.